1. 서 론
2. 수치해석 방법
2.1 배관 유동 해석의 지배방정식 및 수치해석 방법
2.2 배관 유동의 경계 조건 및 수치해석 격자
2.3 벽면 화학반응 조건
3. 수치해석 결과
3.1 배관 입구와 출구의 압력 차에 의한 퍼지의 영향
3.2 배관의 작동 압력에 따른 퍼지의 영향
3.3 배관 벽면 온도에 따른 퍼지의 영향
4. 결 론
1. 서 론
반도체 배출 공정 중 배관 내부의 잔류 화학물질은 작업자나 공기중에 노출될 경우 매우 위험하다[1,2]. 퍼지는 배관 내부의 잔류 화학물질을 제거하기 위해 불활성 기체를 주입하여, 배관 내부 잔류 가스를 저감하고 작업자의 위험을 줄여주는 제어 방법이다[3]. 퍼지 수행 시 배관의 구조, 부산물(by-product)과 기체의 화학반응, 내부 화학물질 구성 등을 고려하여 최적 조건을 확인하기 위해서는 배관 내부의 유동 해석과 화학적 물리적 반응에 대한 이해가 필요하다. 배관 내부의 상세한 유동 현상, 화학반응 등은 실험적으로 측정하거나 가시화가 어려워 수치해석 방법이 필수적이다.
연속체 가정하에서는 Navier-Stokes 방정식을 수치해석 방식을 통해 해를 얻을 수 있다. 그러나, 진공의 영역을 다루는 반도체 공정에서는 수치해석 기법이 달라진다. 저진공 영역의 경우 벽면에서의 no-slip 조건을 만족하지 않고, 고진공 영역의 경우 연속체 가정이 성립하지 않아 Navier-Stokes 방정식을 활용한 수치해석이 불가능하다. 그렇기에 flow regime에 따른 올바른 경계 조건과 해석자의 선택이 중요하다.
반도체 공정의 특성상 배관 유동은 저진공에서 고진공까지 다양한 진공 영역이 존재한다. 누센 수(Knudsen number)는 유체 입자 간 평균 자유 거리(mean free path)와 유체가 흐르는 배관의 지름 혹은 형상의 길이 규모(length)의 비로 정의되며, 유체의 희박함을 나타내는 척도 중 하나이다. 누센 수에 따라 그 값이 10 이상이면 자유 분자 흐름(free-molecular flow), 0.1~10 사이의 값을 가지면 천이 유동(transition flow), 0.001~0.1의 값을 가지면 미끄럼 유동(slip flow), 0.001보다 작으면 연속체 유동(continuum flow)이다[4]. Navier-Stokes solver의 경우 연속체 유동의 영역에서의 no-slip condition과 미끄럼 유동에서의 slip-boundary condition을 통해 수치해석 방법을 적용할 수 있지만, 자유 분자 흐름 영역에 가까워질수록 연속체 가정이 성립하지 않아 이를 적용할 수 없다. 이렇듯 진공 영역의 Navier-Stokes solver의 경우 누센 수에 따른 올바른 경계 조건 선택이 중요하다.
본 연구에서는 이러한 누센 수 영역을 고려하여 배관 내부 퍼지 및 중성화 과정을 시뮬레이션하고 현상을 이해하고자 하였다. 배관의 입구와 출구의 압력 차이, 배관의 작동 압력 및 벽면의 온도에 따른 퍼지 시간을 시뮬레이션하여 최적의 퍼지 상황을 찾고자 하였다.
2. 수치해석 방법
2.1 배관 유동 해석의 지배방정식 및 수치해석 방법
본 연구에서는 연속체 유동 및 미끄럼 유동 영역에서의 벽면 화학반응을 고려한 유동을 해석하기 위해 상용 소프트웨어인 ANSYS FLUENT(2021 R1)를 사용하였다. 지배방정식으로는 질량보존방정식, 운동량방정식, 에너지방정식, 화학종 및 벽면 화학반응 해석을 위한 종수송방정식을 활용하였다.
이때, 는 종 의 local mass fraction이며, 는 diffusion term, 는 volumetric reaction에 의한 종 의 변화를, 는 dispersed phase에 의한 변화를 나타낸다. , 𝜌와 는 각각 시간, 밀도, 속도를 나타낸다. 벽면에서의 화학반응은 다음과 같은 벽면 화학반응을 고려하여 나타낼 수 있다[5,6,7].
, , , , , 는 gas, bulk, site species의 화학 계수를, , , 는 gas, bulk, site species를, , 는 forward rate constant와 backward rate constant를 의미한다. 배관 벽면에서 반응계수를 고려한 반응 속도는 다음과 같이 정의된다.
와 는 각각 번째 gas species와 번째 site species의 molar concentration을 의미하며, , , , 는 각종의 rate exponent를 의미한다. , , 는 반응을 통해 생성되거나 사라지는 번째 gas species, 번째 bulk species, 번째 site species의 net molar rate이다. 식 (3), 식 (4), 식 (5)을 계산할 때는 반응 속도가 bulk 종의 농도에 영향을 받지 않는다고 가정한다.
2.2 배관 유동의 경계 조건 및 수치해석 격자
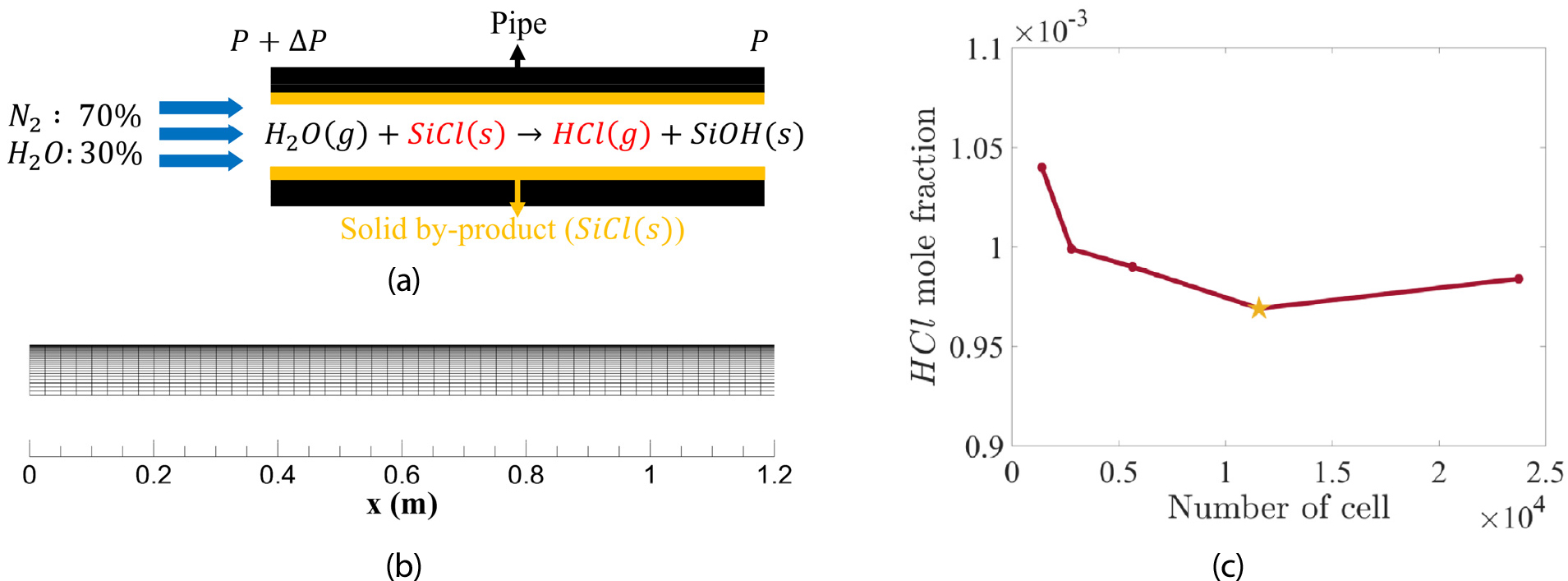
본 연구에서는 배관을 2D axisymmetric으로 가정하였다. 배관의 지름은 16 cm이며 길이는 10 m이다. 계산에 사용된 격자는 주유동 방향과 반지름 방향으로 각 400개, 30개이다. Fig. 1(a)는 시뮬레이션의 경계 조건에 대한 그림이다. 배관의 입구에서는 pressure inlet 조건을 적용했으며, 70%의 질소와 30%의 수증기가 배관에 들어온다. 벽면에서는 가 일정하게 분포되어있다고 가정하였으며 벽면 부산물의 두께는 무시하였다. 배관의 출구에서는 pressure outlet 조건을 적용했으며, 배관의 유동은 laminar를 가진다고 가정하였다. Fig. 1(b)는 계산에 이용된 격자의 해상도이다. 배관의 길이가 매우 길어 전체 길이 10 m 중 1.2 m만 나타냈으며, 그림과 같은 균일한 격자를 시뮬레이션 배관 전체에 사용하였다. Fig 1.(c)는 격자 수렴성에 관한 그래프이다. 격자의 수렴성은 평균 의 몰분율을 기준으로 판단하였다. 배관의 입구와 출구, 벽면에서의 경계 조건의 값은 Table 1, Table 2, Table 3과 같다. Table 2의 Operating pressure case study의 경우 50 Pa, 25 Pa의 누센 수 영역이 미끄럼 유동이므로 slip-boundary 경계 조건을 사용했다. 이때, 500 Pa, 250 Pa, 50 Pa, 25 Pa에 해당하는 누센 수는 각각 0.000269, 0.000537, 0.002686, 0.005319이며, 특성 길이는 배관의 지름으로 설정하였다. Table 1의 경우 배관의 입구와 출구의 압력 차에 따른 퍼지의 경향을 알아보고자 하였으며, Table 2는 작동 압력에 따른 퍼지의 경향을, Table 3은 벽면 온도에 따른 퍼지의 경향을 알아보았다.
Table 1.
Boundary condition for inlet pressure case study
| Inlet pressure | Outlet pressure | Wall temperature | |
| I | 500.5 Pa | 500 Pa | 800 K |
| II | 500.3 Pa | 500 Pa | 800 K |
| III | 500.1 Pa | 500 Pa | 800 K |
Table 2.
Boundary condition for operating pressure case study
| Inlet pressure | Outlet pressure | Wall temperature | |
| I | 500.5 Pa | 500 Pa | 800 K |
| II | 250.5 Pa | 250 Pa | 800 K |
| III | 50.5 Pa | 50 Pa | 800 K |
| IV | 25.5 Pa | 25 Pa | 800 K |
Table 3.
Boundary condition for wall temperature case study
| Mass flow inlet | Outlet pressure | Wall temperature | |
| I | 500.5 Pa | 500 Pa | 900 K |
| II | 500.5 Pa | 500 Pa | 800 K |
| III | 500.5 Pa | 500 Pa | 700 K |
| IV | 500.5 Pa | 500 Pa | 600 K |
2.3 벽면 화학반응 조건
벽면 화학반응은 식 (8)과 같다. Wise[8]의 실험데이터로부터 pseudo-first order reaction을 가정하고 구한 pre-exponential factor 는 이며, 활성화 에너지 는 이다. 벽면 화학반응의 계산 초기조건으로 이 배관 벽면에 고르게 분포되어있다고 가정했기에 surface coverage 값을 1로 설정하였으며, site density는 이다.
퍼지의 경향은 벽면에서의 이 제거되는 시간과 배관 내부의 의 몰분율의 변화를 통해 확인하였다. 퍼지 시간은 이 사라지고, 배관 내부의 평균 의 몰분율이, 평균 몰분율의 최댓값의 0.2%가 되는 시간을 기준으로 하였다.
3. 수치해석 결과
3.1 배관 입구와 출구의 압력 차에 의한 퍼지의 영향
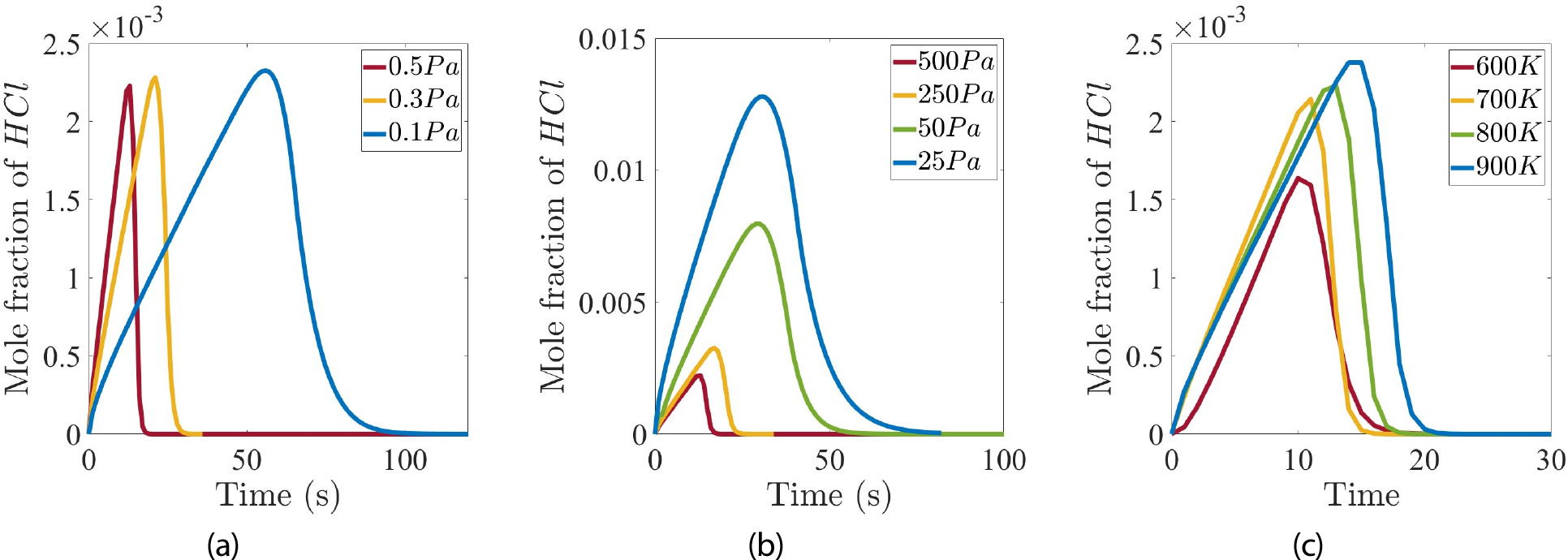
Fig. 2(a)는 입구와 출구의 압력 차에 의한 퍼지의 영향을 확인하기 위한 그래프로, 전체 배관에 대한 평균 의 몰분율(mole fraction)을 시간에 대해 그린 그래프이다. 압력 차가 클수록 퍼지 시간이 짧아지고, 의 몰분율의 최댓값이 미세하게 감소하는 것을 확인할 수 있었다. Table 4는 압력 차에 따른 질량유량 및 퍼지 시간을 나타낸다. 질량유량은 압력 차가 커질수록 값이 커지며, 질량유량이 커질수록 벽면 화학반응이 활발하게 일어나게 된다. 이는 이 제거되는 시간을 앞당기고, 이 생성되는 시간을 빠르게 하여 퍼지 시간을 앞당기게 한다. 또한, 배관 내의 속력이 빨라져 이 빠져나가는 데 걸리는 시간이 감소한다. 반면, 낮은 압력 차의 경우 질량유량이 감소하게 되면서 이 제거되는 시간이 늘어나고, 상대적으로 오랜 시간 동안 벽면 화학반응이 일어나기 때문에, 오랜 시간 동안 이 생성되게 된다. 이에 따라 몰분율의 최댓값이 증가하게 되며, 퍼지 시간도 늘어나게 된다.
Table 4.
Purging time of inlet pressure case study
| Pressure difference | Mass flow rate() | Removal of | Purge |
| 0.5 Pa | 4.22 | 16 s | 19 s |
| 0.3 Pa | 2.54 | 25 s | 31 s |
| 0.1 Pa | 0.85 | 66 s | 101 s |
압력 차가 낮아질수록 의 몰분율이 최댓값을 갖는 시간과, 이 최댓값을 가지는 시간에서 퍼지가 되는데 걸리는 시간의 차이가 증가하였다. 낮은 압력 차를 가지는 경우, 낮아진 질량유량으로 인해 화학반응이 오랫동안 일어나게 되면서 이 배관에 더 넓게 퍼져있게 된다. 또한, 배관의 속도가 감소하면서 이 빠져나가는 시간이 늘어나게 되면서 이와 같은 시간의 차이를 증가시킨 것으로 판단된다. 낮아진 질량유량은 몰분율 그래프의 개형에도 영향을 주었다. 질량유량이 낮은 경우 벽면에서의 화학반응이 느리게 일어나기 때문에 부드러운 그래프 모양을 가졌으나, 질량유량이 높은 경우 순간적으로 발생하는 의 양이 많아 그래프가 급격하게 증가하고 감소하게 되면서 날카로운 개형을 가지게 되었다.
배관의 평균 속력은 입구와 출구의 압력 차가 0.5 Pa, 0.3 Pa, 0.1 Pa일 때, 1.487 m/s, 0.892 m/s, 0.298 m/s로 압력 차가 감소할 때마다 배관 유동의 평균 속력이 약 0.6 m/s만큼 일정하게 감소하는 것을 확인할 수 있었다. 그러나 퍼지 시간은 압력 차가 감소할수록 급격하게 증가하였다. 이는 배관이 낮은 압력 차를 가지는 경우 질량유량이 감소하게 되면서 벽면에서의 화학반응이 느리게 일어나게 되고, 발생한 이 느리게 빠져나가게 되면서 퍼지 시간이 증가한 것으로 판단된다.
3.2 배관의 작동 압력에 따른 퍼지의 영향
Fig. 2(b)는 시간에 따른 배관 내의 평균 의 몰분율 그래프이다. 작동 압력이 낮을수록 낮아진 질량유량으로 인해 이 제거되는 시간이 지연되면서, 의 몰분율이 최댓값을 가지는 시간이 지연되는 것을 확인할 수 있다. 의 최댓값은 작동 압력이 낮을수록 증가하였다. 작동 압력이 낮은 경우 벽면 화학반응이 천천히 일어나게 되면서, 이 생성되는 시간이 길어지게 된다. 그렇기에 배관에 존재하는 의 상대적인 양은 증가하게 된다. 반면, 작동 압력이 높은 경우 높은 질량유량으로 인해 벽면 화학반응이 빠르게 일어나면서 이 제거되는 시간이 앞당겨지게 된다. 이 경우 이 생성되는 시간이 감소하게 되면서 배관에 존재하는 의 상대적인 양이 감소하게 된다.
작동 압력이 낮아질수록 몰분율 그래프의 개형이 넓고 부드러운 형상을 가졌다. 몰분율의 최댓값은 이 배관을 빠져나가기 시작하는 시간과 관련된다. 질량유량이 낮아지면 화학반응이 긴 시간 동안 일어나게 되기 때문에, 배관 내에 이 넓게 퍼져있게 된다. 그로 인해 몰분율이 최댓값을 가진 시간 이후에도 이 배관을 빠져나가는 데 오랜 시간이 걸리게 되며, 상대적으로 부드럽고 넓은 형상의 몰분율 그래프 개형을 가지게 된다. 반면, 작동 압력이 이 급격하게 생성되기 때문에 배관 내 좁은 영역에 이 분포하게 되며, 이 배관을 빠져나가는 시간도 짧아지게 된다. 이는 몰분율 그래프가 상대적으로 날카롭고 좁은 그래프 개형을 가지게 한다.
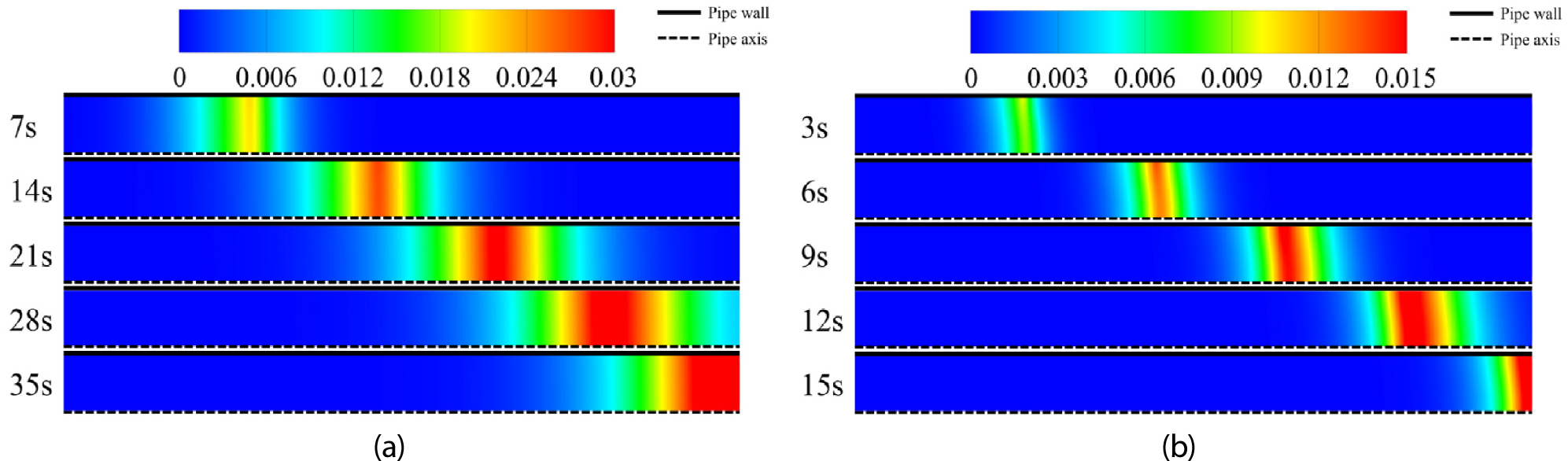
Fig. 3(a)와 Fig. 3(b)는 시간에 따른 의 몰분율 변화를 나타낸다. 작동 압력이 낮을수록 이 배관 내에 더 넓게 분포해있으며, 퍼지에 오랜 시간이 걸리는 것을 확인할 수 있었다. 작동 압력이 낮아질수록 벽면에서 slip velocity를 가지게 되면서 배관 중심부와 벽면의 속도 차이가 줄어들게 되며, 배관 중심부와 벽면의 몰분율 분포가 일정하게 되는 것을 확인할 수 있다. 또한, 이 화학반응이 발생하는 부근을 중심으로 뭉쳐서 이동하는 것을 확인할 수 있었다. 이는, 높은 벽면 온도로 인해 이 배관에서 퍼져나가는 시간보다, 높은 아레니우스 상수로 인해 벽면에서 이 발생하는 양이 많아 생기는 현상으로 판단된다. 작동 압력이 낮을수록 이 뭉쳐있는 정도가 약해졌으며, 이는 퍼지 시간을 지연시켰다. 반대로 작동 압력이 높을수록 이 뭉치는 정도가 강해졌고 퍼지 시간을 줄일 수 있었다.
Table 5는 배관의 작동 압력에 따른 질량유량 및 퍼지 시간을 나타낸다. 배관의 평균 속력은 작동 압력이 500 Pa, 250 Pa, 50 Pa, 25 Pa일 때 각각 1.487 m/s, 1.491 m/s, 1.510 m/s, 1.528 m/s로 배관의 작동 압력이 낮아질수록 속력이 미세하게 증가하였다. 그러나, 배관의 속력이 높을수록 퍼지 시간을 앞당기지는 못했다. 벽면 화학반응을 고려해야 하는 퍼지의 경우, 배관 내 을 제거해야 할 뿐만 아니라 화학반응을 통해 벽면에 부착되어있는 부산물을 제거해야 한다. 그렇기에 효율적인 퍼지 조건을 고려하기 위해서는, 벽면 화학반응을 고려할 수 있는 질량유량과 퍼지 시간의 관계를 알아보아야 함을 시사한다.
Table 5.
Purging time of operating pressure case study
| Operating pressure | Mass flow rate() | Removal of | Purge |
| 500 Pa | 4.22 | 16 s | 19 s |
| 250 Pa | 2.12 | 22 s | 26 s |
| 50 Pa | 0.44 | 38 s | 62 s |
| 25 Pa | 0.23 | 41 s | 82 s |
3.3 배관 벽면 온도에 따른 퍼지의 영향
Table 6에 나와 있듯이 배관의 벽면 온도가 높아지는 경우, 배관의 질량유량이 감소하였다. 또한, 벽면의 특정 온도보다 높은 경우 퍼지 시간이 지연됐다. 의 제거시간과 퍼지 시간은 700 에서 최솟값을 가졌다. 벽면 온도가 낮은 경우 아레니우스 상숫값이 낮아서 벽면 화학반응이 느리게 일어났고, 이는 퍼지 시간이 지연되는 요인이 되었다. 반면, 벽면 온도가 특정 온도보다 높은 경우 아레니우스 상숫값은 높았지만, 질량유량이 낮아지면서 이 제거되는데 걸리는 시간이 증가하였다. 이와 같은 결과를 통해 질량유량이 퍼지에 큰 영향을 준다는 것을 알 수 있었으며, 질량유량과 벽면 온도를 고려하면 최적의 퍼지 시간을 계산할 수 있을 것으로 판단된다.
Table 6.
Purging time of wall temperature case study
| Wall temperature | Mass flow rate() | Removal of | Purge |
| 900 K | 3.45 | 18 s | 22 s |
| 800 K | 4.22 | 16 s | 19 s |
| 700 K | 5.31 | 14 s | 16 s |
| 600 K | 6.93 | 20 s | 20 s |
Fig. 2(c)는 배관 벽면의 온도에 의한 퍼지의 영향을 확인하기 위한 그래프로, 전체 배관에 대한 평균 의 몰분율을 시간에 대해 그린 그래프이다. 벽면 온도가 증가할수록 몰분율의 최댓값이 증가했으며, 최댓값을 가지는 시간도 지연되었다. 600 K과 700 K의 경우 의 몰분율이 최댓값을 가지는 시간은 비슷했으나, 최댓값의 크기에는 차이가 있었다.
700 K의 벽면 온도를 가지는 경우 아레니우스 상수는 로 반응 속도가 매우 빠르며 입구에서의 수증기가 배관 벽면에 닿은 순간 이 제거되었다. 그렇기에, 의 몰분율이 최댓값을 가지는 시간과 이 제거되는데 걸리는 시간이 비슷하였다. 반면, 600 K의 벽면 온도를 가지는 경우 아레니우스 상수는 700 K에 비해 약 100배 작은 이였으며 수증기가 배관 벽면에 닿아도 이 제거되는 데 시간이 오래 걸렸다. 그렇기에 의 몰분율이 최댓값을 가지는 시간 이후에도 화학반응이 계속 발생했으며, 이 제거되는 시간과 이 제거되는 시간이 비슷하였다. 이는 벽면 온도가 700 K일 때 보다 작은 의 최댓값을 가지게 하였으며 퍼지 시간을 지연시키는 원인으로 작용하였다. 900 의 경우 최대 몰분율 값이 가장 큰 값을 가졌다. 높은 온도로 인해 아레니우스 상수가 컸고, 이에 따라 순간적으로 생성되는 의 상대적인 양이 많아 최댓값이 가장 큰 값을 가지는 것을 알 수 있다. 그러나 질량유량이 낮아 이 제거되는 데 오랜 시간이 소요되었고, 퍼지 시간도 증가하였다.
4. 결 론
본 연구에서는 배관의 입구와 출구의 압력 차, 작동 압력, 벽면 온도에 따른 퍼지 시간과 이에 따른 배관 유동의 특성을 확인하였다. 배관의 압력 차가 클수록 퍼지 시간이 감소하고 몰분율의 최댓값이 감소하는 경향을 보였다. 반대로, 압력 차가 작아질수록 퍼지 시간이 오래 걸렸으며 몰분율의 최댓값이 미세하게 증가하는 경향을 확인할 수 있었다. 배관의 작동 압력이 낮아질수록 퍼지 시간은 증가하였고, 몰분율의 최댓값이 증가하였다. 또한, 낮은 작동 압력을 가지는 경우 몰분율 그래프가 넓고 부드러운 개형을 가졌다. 배관의 벽면 온도가 낮아지는 경우 낮아진 아레니우스 상수로 인해 벽면에서의 화학반응이 느리게 일어났고, 이에 따라 퍼지 시간이 증가하였다. 반면, 벽면 온도가 높아지는 경우 몰분율의 최댓값이 증가하였고, 최댓값을 가지는 데 걸리는 시간이 지연되는 경향을 보였으며 퍼지 시간 또한 증가하였다. 이는 낮아진 질량유량으로 인해 벽면에서의 화학반응이 느리게 일어나게 되면서 생긴 현상으로 판단된다.
이러한 결과들을 종합해볼 때 최적의 퍼지 조건은 질량유량에 매우 지배적인 것으로 판단된다. 배관의 유속을 고려하는 것은 배관 내 유해한 가스를 제거할 때는 최적의 퍼지 조건을 고려하는 변수로서 유용하게 작용한다. 그러나, 벽면 화학반응을 고려해야 하는 퍼지의 경우 화학반응의 속도를 고려해야 했기 때문에 적합하지 않았다. 또한, 벽면 화학반응이 활발하게 발생하기 위해 배관 벽면의 온도를 높이는 것은 아레니우스 상수를 높여 퍼지 시간을 앞당길 수 있었지만, 일정한 온도 이상에서는 낮아진 질량유량으로 인해 오히려 퍼지 시간이 지연되었다.